
目前,我们对原子结构的理解建立在量子理论和波动力学发展的基础上。大约在 1900 年以前,大量由各种原子发射的具有一系列特征谱线的光谱资料、热辐射对频率的依存关系以及光电子发射现象的特点都不能用经典连续介质物理给出满意的解释。普朗克在1900 年对热辐射作了成功的解释,他提出辐射是以能量子或光子为单位不连续发射的,光子具有的能量为hr。爱因斯坦在1905 年用同一个概念解释了光发射现象。1913年,玻尔提出子一个原子模型,认为电子只能在某些稳定的轨道中运动(没有辐射),并假设当电子在这些具有稳定能量状态的轨道之间跃迁时就会发射或吸收光量子而产生光谱线。这个观点可以对实验中观察到的光谱线系列给出满意的解释。
玻尔原子
玻尔原子中,量子理论要求电子的角动量必须是h/2T 的整数倍,与h/2T 相乘的整数n 称为主量子数。随着几的增加,电子的能量增加,同时电子离开带正电荷的原子核也更远。除了主量子数,电子还由其他一些量子数来描述:L是衡量轨道偏心度的量子数,其值可在0到n-1之间变动;m是衡量椭圆轨道的空间取向的量子数,其值取-l到+1之间的整数;s标志电子自旋的方向是正向或反向。随着n及l的增加,通常电子轨道的能量也增加。
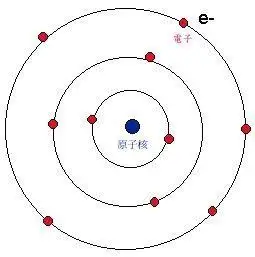
玻尔原子结构示意图
对原子结构的另一个限制是泡利不相容原理,即在任何一个原子中任意两个电子不可能具有完全相同的量子数。当原子中电子数增加时,增加的电子就去填充主量子数较大的较高能态的轨道。按照泡利不相容原理可以依次确定各轨道所能安置的电子数,从而决定元素的周期分类。
电子轨道
虽然在定量解释很多光谱数据方面取得了成功,玻尔原子模型仍然不能说明一些电子轨道的稳定性和光谱线的精细结构。德布罗意在1924年提出的光的二象性是普遍适用的。所谓光的二象性,指的是所观察到的光现象既可以从波动性也可以从光子的能量和动量出发加以讨论。根据普朗克方程和德布罗意方程,任何粒子的运动都和一定频率及波长的波动现象相联系,这些关系已经被X射线、电子及中子衍射实验所证实。稳定的电子轨道不应该出现相消干涉,而当轨道的周长为波长整数倍时就会产生驻波。
原子间的键
形成稳定无机晶体的主要作用力是正负离子间的静电引力(如KCI)以及由于两个原子间共有电子对而形成的电子结构的稳定性。
离子键
离子键的本质可以用 KCI 的生成来说明。当将一个中性的钾原子电离成K+时,消耗电离能4.34eV。而一个中性的氯原子获得一个电子变为CI-时,可得到电子亲和势 3.82 eV。这就是说,将两者离子化时需要净消耗0.52 eV的能量。
共价键
稳定氢分子H2的形成情况和刚才讨论过的KCl的情识很不一样,这里我们考虑当两个氢原子靠近时的情况。每个氢原子有一个1s电子。当电子远离质子时势能为0,而在每个质子附近有最小值。沿两个质子间连线,电子的势能增加,但它总是较自由电子时的势能为低。当核靠近时,沿两个质子间连线发现电子的几率较大,而最稳定的情况为哑铃状分布。当两个质子更加接近时,质子问由于电子云密度增大而导致的能量增益进一步增加,但是同时斥力也增加了,从而导致了一个能量最小值。导致总能量最小的这一电子分布或波函数是系统的稳定态。一对电子形成一个稳定的键,因为只有两个电子可以列入能量最低的波函数(不相容原理)。第三个电子就要进入能量较高的量子态,结果系统就不稳定。

范德瓦耳斯键
在原子回或分子间另外一种弱的静电力称为范德瓦耳斯力或色散力。任何原子或分子都存在一个波动着的偶极矩,它随着电子的瞬时位置而变动。这个偶极矩的电场会诱导邻近原子产生偶极矩,这个诱导偶极矩与原始偶极矩的相互作用产生一种吸引力。这种情况下的键能比较弱(约0.1eV),但在惰性气体及没有其他结合力的分子间,这种力就变得重要起来了。
金属键
金属原子间的内聚力是由原子聚集体中的量子力学效应产生的。
中间键型
虽然KCI 结构可以看成近乎是完全离子型的,而H2是完全共价型的,但还有很多中间型。这种中间型的特点是既具有离子的电子构型,又在沿原子中心间的连线上具有较大的电子浓度。
粉体圈整理
了解优质装备供应商,请联系客服18666974612(微信同号)
